热文:2019九江二模各科试题及答案汇总附高考解题方法
向学霸进军汇总收拾2019九江二模各科试题及谜底,考题由驰名专家结合了2019高考大纲(测验说明)并依托最新时势为配景出的,通过这次考试,高三的考生可了解本身的温习备考情况,同时也能够作为2019高考温习资料。

2019九江二模各科试题及谜底目次一览
2019九江二模(语文科目)试题及答案
2019九江二模(数学科目)试题及答案
2019九江二模(英语科目)试题及谜底
2019九江二模(物理/化学/生物)试题及谜底
2019九江二模(地舆/汗青/政治)试题及答案

附:卤族方面试题的解题要领与才力
卤素及其化合物与化工临盆、一般生涯、科学手段等方面有着普遍的关联,如氯碱家产、漂白粉应用、饮用水消毒、情形保护等,是近几年高考命题的热点。预计2018年高考仍会以与氯气及其化合物的知识有关的化工出产、科学手段等方面为载体,联合氧化还原回响、离子反响、化学尝试方案规划进行相干考察,考查学生分析管理问题的才智和对知识的应用才力,并同时强化化学常识与生活、社会现实问题的联系,此类题设问新颖,与生涯、社会实际标题联合细密,且赋分值较高,复习时注意这方面的知识。
一、新制氯水的成分及相关性质
1、氯水的成分:Cl2溶于水:Cl2+H2O⇌H++Cl-+HClO
三种分子:Cl2、H2O、HClO;四种离子:Cl-、H+、OH-、ClO-
2、氯水的性子:氯水的多种身分信心了氯水的化学性质表现出多样性:
(1)Cl2的强氧化性;
(2)HCl的强酸性;
(3)HClO的强氧化性、弱酸性和不镇静性;
(4)Cl-的性质:
方法才力:
1、氯水的多种成分信念了氯水的化学性质表现出多样性:Cl2的强氧化性;HCl的强酸性;HClO的强氧化性、弱酸性和不镇静性;Cl-的性子。在差异的反响中,氯水起感化的成分差异,现列表如下:

2、新制氯水、久置氯水、液氯的角力
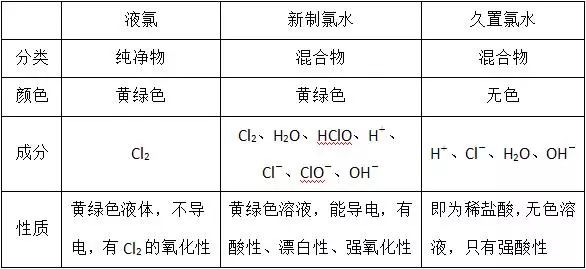
二、氯气的制备及相关尝试切磋
1、试验装置:
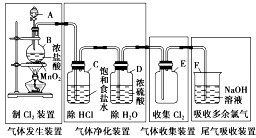
2、制取过程
(1)反映原理:用强氧化剂(如KMnO4、K2Cr2O7、KClO3、MnO2等)氧化浓盐酸,譬喻MnO2+4HCl(浓)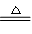 MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)试剂:二氧化锰和浓盐酸。
(3)净化方法:用饱和食盐水除去HCl,再用浓硫酸撤消水蒸气。
(4)收集方法:向上排氛围法或排饱和食盐水法。
(5)尾气吸收反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O。
(6)验满要领:
①将潮湿的淀粉-碘化钾试纸靠近盛氯气的瓶口,迟疑到试纸立即变蓝色,则证明已集满;
②将湿润的蓝色石蕊试纸靠近盛氯气的瓶口,旁观到试纸立即孕育先变红后褪色的变化,则证实已集满;
③凭据氯气的颜色鉴定是否收集满。
(1)一套完备的制取气体的实验装配搜罗四个部分:孕育装置→净扮装置→网络或性子验证装配→尾气措置装配。
(2)正确闻气体气味的要领:取一只盛满气体的集气瓶,轻微打开玻璃片,用手在瓶口轻轻扇动,使极少量的气体飘进鼻孔,闻气体的气味。
(3)必需用浓盐酸,MnO2与稀盐酸不反应。
(4)为了镌汰制得的Cl2中HCl的含量,以是加热温度不宜过高,裁减HCl的挥发。
(5)尝试结束后,先使反响制止并排击残留的Cl2,再拆缷装置,停止污染气氛。
(6)尾气吸收时,不及用澄清石灰水接收Cl2,因为溶液中Ca(OH)2浓度小,接收不完全。
三、卤素单质性子的递变性、相似性和特别性
1、物理性子:Br2是一种深红棕色液体,易挥发;I2是一种紫玄色固体,易升华。Br2溶解在水中的颜色是黄色→橙色,I2消融在水中的颜色是深黄色→褐色,Br2消融在CCl4中的颜色是橙色→橙赤色,I2溶解在CCl4中的颜紫色→深紫色。
2、化学性子相似性:
(1)都能与大多数金属反映:2Fe+3Br2=2FeBr3;I2+Fe=FeI2;
(2)都能与H2回响:H2+X2=2HX;
(3)都能与H2O反响:X2+H2O⇌HX+HXO(F2破例);
(4)都能与碱液回响:X2+2NaOH=NaX+NaXO+H2O(F2例外)。
1、F2、Br2、I2的特别性:
(1)Br2是常温下独一呈液态的非金属单质;液溴易挥发且有毒,通常用水液封来生存。
(2)I2易升华,I2遇淀粉变蓝。
(3)Br2和I2都可被某些有机溶剂(如四氯化碳、汽油苯)萃取。
(4)氟元素无正价,F2与H2O孕育置换回响天生O2(2F2+2H2O=4HF+O2),F2与Xe、Kr等有数气体可回响生成白色氟化物。
(5)I2易与Na2S2O3溶液回响:I2+2S2O3
2-
=2I-+S4O6
2-
,用于经由滴定(以淀粉为指示剂)来定量测定碘的含量。
2、Cl-的检修:白色沉淀,含Cl-。

检验卤素离子时加入稀硝酸是为了防止CO3
2-
等离子的干扰。
3、能使溴水褪色的物质:
(1)被H2S、SO2、SO3
2-
、I-等还原剂还原而褪色。
(2)与NaOH等强碱溶液孕育自身氧化还原反响而褪色:Br2+2NaOH=NaBrO+NaBr+H2O。
(3)与较活泼金属(如Mg+Br2=MgBr2)反响而褪色。
(4)能与溴发生加成回响的不饱和烃及其衍生物,如烯烃、炔烃等。
(5)能被溴水氧化的、含有醛基的化合物。
(6)能与溴水产生反映的碱性物质,如Na2CO3等。
(7)插足活性炭等吸附剂,使溴水褪色。
本文由民众号《向学霸进军》整顿编纂于收集返回搜狐,查察更多
责任编辑:
特荐文章

点击排行
头条文章
热点推荐